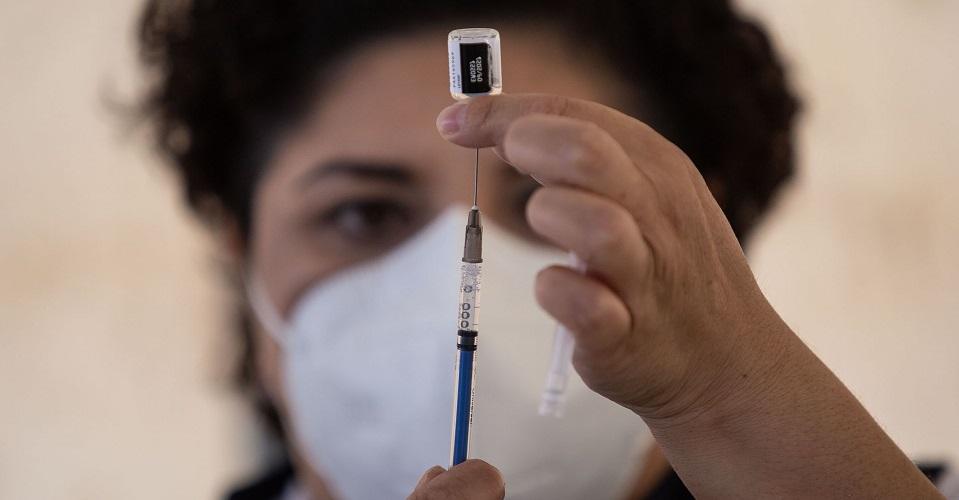
Comité de expertos de Cofepris recomienda aplicar vacuna COVID de Pfizer a mayores de 12 años
El Comité de Moléculas Nuevas de la Comisión Federal para la Protección contra Riesgos Sanitarios (Cofepris) recomendó autorizar el uso de la vacuna contra COVID-19 de Pfizer en población de 12 años y más.
El subsecretario de Salud, Hugo López Gatell, informó, a través de un tuit, que en caso de autorizarse la vacuna a personas partir de esta edad, la Secretaría se preparará para incluirlos en el Plan Nacional de Vacunación.
Esto no es todavía la autorización para uso de emergencia que se está otorgando a las vacunas en muchos países del mundo y a través de diversas agencias sanitarias, es un paso previo, pero un paso fundamental.
Comité de Moléculas Nuevas emite opinión favorable para ampliar uso de emergencia de vacuna Pfizer-BioNTech a partir de los 12 años.
Conoce los resultados https://t.co/o8XM5dSjQ9
Conoce el proceso de optimización https://t.co/gxqqRaZmn3 pic.twitter.com/IVzpitRdDn— COFEPRIS (@COFEPRIS) June 11, 2021
Dos órganos auxiliares de consulta y opinión a solicitudes relacionadas con medicamentos y demás insumos para la salud –el Comité de Moléculas Nuevas (CMN) y Subcomité de Evaluación de Productos Biotecnológicos (SEPB)- sesionaron este 11 de junio para emitir una opinión técnica sobre la ampliación del grupo etario a partir de los 12 años, para la aplicación de la vacuna BNT162b2 (Pfizer-BioNTech COVID19 vaccine). La opinión fue favorable por unanimidad.
Esta decisión forma parte del proceso de aprobación necesario para el cumplimiento de los requisitos de calidad, seguridad y eficacia, indispensable al considerar un producto.
El CMN y el SEPB no autorizan o rechazan moléculas; emiten una opinión técnica favorable o no favorable basada en la evidencia científica y médica presentada, misma que los laboratorios integran a sus expedientes presentados ante la Comisión de Autorización Sanitaria.
La instancia queda ahora pendiente de la solicitud de ampliación de grupo etario de la vacuna BNT162b2 (Pfizer- BioNTech COVID19 vaccine).
La vacuna de Pfizer y BioNTech tiene ya la autorización de uso de emergencia en niños de hasta 12 años en Europa, Estados Unidos, Canadá, Brasil y Chile.
De hecho desde mayo, la Administración de Alimentos y Medicamentos de los Estados Unidos (FDA) autorizó el uso de esta vacuna, en Estados Unidos, en menores de 12 a 15 años.
