
“Uno de los capítulos más emocionantes del libro de la vida”: cómo descifrar los misterios del genoma humano está cambiando el mundo por completo

Este mes se cumplieron 15 años desde que la secuencia completa del genoma humano fue publicada por primera vez, lo que anunciaba una nueva era para la medicina.
Desde entonces, la tecnología ha acelerado de forma notable la secuenciación genómica y ha reducido su costo. Pero ¿hasta qué punto se han materializado los tan esperados avances médicos?
"Nos hemos embarcado en uno de los capítulos más emocionantes del libro de la vida", dijo el profesor Allan Bradley, director del Instituto Wellcome Trust Sanger, al celebrar el éxito del proyecto del Genoma Humano.
Completar la secuencia del genoma humano requirió 10 años de trabajo y la inversión de unos US$30.000 millones. Ahora, los avances en la capacidad de las computadoras han hecho caer el costo de secuenciar el genoma humano por debajo de los US$500.
Un empresa llamada Oxford Nanopore incluso ha desarrollado un lector portátil, del tamaño de un celular, que permite secuenciar material genético en cuestión de minutos.
El doctor Gordon Sanghera, director ejecutivo de la empresa, habla sobre la posibilidad de crear "el internet de las cosas vivas, a través de una conexión en tiempo real con la información del ADN", gracias al uso de ese tipo de aparatos.
Asegura que ese dispositivo no solo tiene aplicaciones en el campo de la salud. También puede servir para establecer el origen de la comida de un restaurant o la presencia de microbios peligrosos en una planta procesadora de alimentos o en las fuentes de agua. También puede utilizarse para analizar rastros de ADN en lugares donde se han cometido delitos.
"Este es el código de barras definitivo", señala.
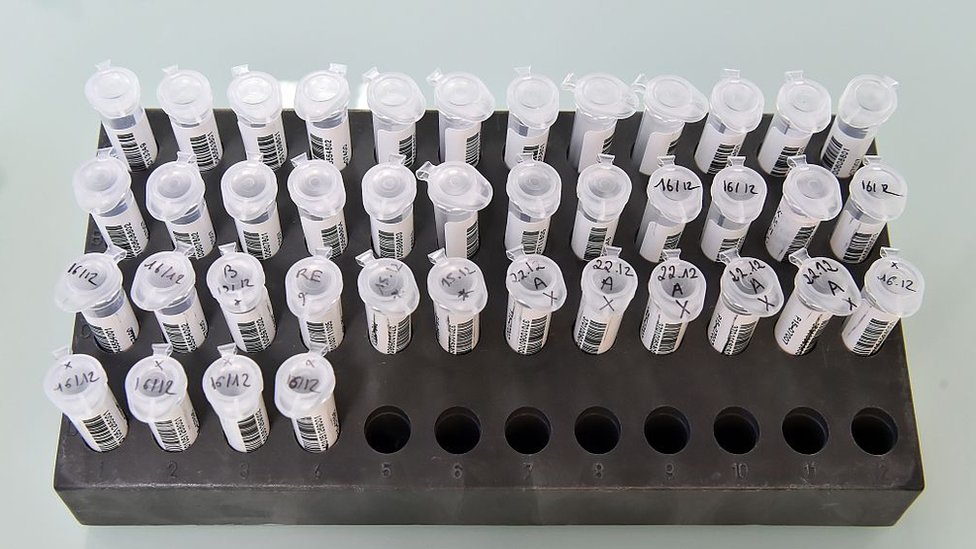
Un cabello humano tiene 10.000 veces el grosor de un filamento de ADN pero el dispositivo portátil, llamado MiniON, lo procesa a través de un mini agujero -conocido como nanoporo- y lee sus señales eléctricas, las cuales son convertidas instantáneamente en una secuencia de ADN.
Sanghera, cuya empresa ya ha captado más de US$600 millones en inversiones, cree que ese aparato podría ser usado en el hogar para diagnosticar infecciones comunes y así reducir las visitas innecesarias al médico y la excesiva prescripción de antibióticos.
Asegura que durante la próxima década, "se secuenciará el ADN de cada recién nacido" con lo que se podrá saber si tiene disposición genética a sufrir enfermedades concretas y, en consecuencia, se podrán tomar medidas preventivas.
Prevención
La reducción en el costo de la secuenciación ha llevado a un rápido aumento en el número de estas.

Illumina, una compañía que presta estos servicios -valorada en US$35.000 millones en el mercado bursátil estadounidense- estima que más de 500.000 genomas han sido secuenciados en todo el mundo.
Pero es la forma cómo esta información será combinada con otros datos y luego analizada lo que está generando entusiasmo.
El Biobank, creado en 2007 en Reino Unido por el Wellcome Trust, ha registrado 500.000 voluntarios que han compartido su información médica de forma anónima con la esperanza de mejorar la prevención, diagnóstico y tratamiento de las enfermedades.
Científicos en el Hospital BWH en Boston, Massachusetts, usaron información del Biobank para subrayar el aumento en el riesgo de desarrollar diabetes de tipo 2 entre quienes trabajan en turnos laborales distintos al horario tradicional de 9 am a 5 pm, como quienes cubren horarios rotativos o trabajan de noche, entre otros.
Los investigadores hallaron que la gente que trabajaba en patrones horarios irregulares tenían 44% más probabilidades de desarrollar diabetes de tipo 2 que quienes trabajan horarios fijos diurnos.
Ahora, la información genética será añadida a la mezcla.
Tratamientos específicos
En abril, el Bionbank anunció planes para hacer la secuenciación genómica completa de 50.000 voluntarios para el año 2019. El proyecto será financiada con un fondo de US$41 millones aportado por el Consejo de Investigación Médica y será llevado adelante por el Instituto Wellcome Sanger en Cambridge.
Un consorcio conformado por varias compañías, encabezado por Regeneron Pharmaceuticals, ya se ha comprometido a leer y analizar los datos del exoma -un pequeño grupo de datos del genoma entero- de los voluntarios. Cada empresa invertirá US$10 millones en el proyecto.
Hay grandes esperanzas de que esa información genética, analizada por sistemas de inteligencia artificial (AI, por sus siglas en inglés), ayude a acelerar el diagnóstico de cáncer y llevará a tratamientos más específicos para combatirlo.

La compañía suiza Sophia Genetics ha desarrollado un sistema de AI que ha sido usado en el diagnóstico de 200.000 pacientes en más de 400 hospitales en 55 países.
"Sophia tiene la capacidad de abrir el camino hacia una inteligencia colectiva que ayudará a diagnosticar y tratar a cada paciente de forma precisa e igualitaria alrededor del mundo", afirma el doctor Jurgi Camblong, uno de los fundadores de la empresa.
Con estos sistemas, miles de millones de datos son analizados en unos pocos minutos. Luego, los resultados son refinados por la comunidad médica, lo que ayuda a que el algoritmo se vuelva más inteligente.
Además, los análisis que antes normalmente necesitaban meses ahora se pueden hacer en cuestión de horas.
"Estamos entrando en una nueva era en la que seremos capaces de agrupar los casos de pacientes con cáncer en cohortes y decidir si el cáncer de un paciente específico se parece al de otro dentro de un grupo de 10.000 pacientes", señala Camblong.
Entonces, los médicos sabrán cuál tratamiento funcionó mejor para ese tipo de persona con ese tipo de cáncer.
Inteligencia artificial
El motor de AI recientemente recibió un nuevo impulso cuando se le añadieron capacidades radiomicas, que es la capacidad de extraer información útil de imágenes médicas como las de los tumores, por ejemplo.
Camblong señala que si tú puedes predecir cómo es probable que se desarrolle un tumor, entonces, puedes tratarlo de forma más efectiva.

"Estamos al inicio de una revolución en la medicina", afirma Ruth March, vicepresidente y jefe de Medicina de Precisión y Genómica en la compañía farmacéutica AstraZeneca.
"Un número creciente de pacientes están siendo tratados con medicinas de precisión debido a la creciente comprensión sobre los impulsores genéticos de la enfermedad. Los pacientes pueden se tratados con las medicinas que tienen más probabilidad de beneficiarles", agrega.
Algunas empresas creen que la vinculación entre genómica y el análisis de otros datos de salud podría ayudarnos a vivir vidas más largas y más saludables.
"Estamos combatiendo la tradición médica en la que esperamos hasta que la gente esté enferma antes de tratarla", afirma el profesor Craig Venter, un pionero del genoma humano y cofundador y director de Human Longevity Inc (HLI), una empresa dedicada a ofrecer toda la "inteligencia médica derivada del análisis de información".
HLI se ha aliado con Amra, un líder mundial en análisis de la composición corporal, para combinar el análisis genómico con el perfil metabólico. El objetivo es darle a los pacientes un conocimiento detallado sobre sus mediciones de grasa y musculatura gracias a un simple escaneo de seis minutos.
Pero los avances impresionantes en la medicina han sido más difíciles de alcanzar de lo que muchos esperaban al inicio de la era genómica.
"La finalización del proyecto del genoma humano trajo mucha esperanza sobre mejoras en la comprensión y en el tratamiento de enfermedades. Pero como suele ocurrir, habíamos subestimado la compleja relación entre el genoma con la enfermedad y la salud", concluye Laxmi Parida de IBM.
Entonces, aunque esto es solo el inicio, en la era del genoma, el cuidado de la salud está cambiando de forma irrevocable.ç
Ahora puedes recibir notificaciones de BBC Mundo. Descarga la nueva versión de nuestra app y actívalas para no perderte nuestro mejor contenido.
